我校附属市中医医院巴乾研究员以共同通讯作者在《Cell》发表研究成果
发布时间:2026.05.02点击:10
4月27日,我校附属市中医医院科技创新中心巴乾研究员团队联合浙江大学医学院张强教授、王福俤教授、闵军霞教授团队和博观生物吴军兵博士团队,在铁死亡调控领域取得重要研究突破,原创性研究论著以“Stabilizing MARCH7 as a ferro-guardian against ferroptosis”为题在国际顶级期刊《Cell》在线发表。该研究成果为铁死亡相关疾病的治疗提供了全新靶点,彰显了中医药在精准调控细胞死亡领域的独特价值。

铁死亡是一种铁依赖性的脂质过氧化驱动的细胞死亡方式,与肿瘤、神经退行性疾病、心肌缺血再灌注损伤等多种重大疾病的发生发展密切相关。长期以来,学界对铁死亡调控的研究主要集中在脂质过氧化和铁代谢过程本身,而对于调控细胞铁含量的上游核心因子,以及导致铁稳态失衡的潜在分子机制,仍存在诸多未知,这也成为制约相关疾病诊疗突破的关键瓶颈。
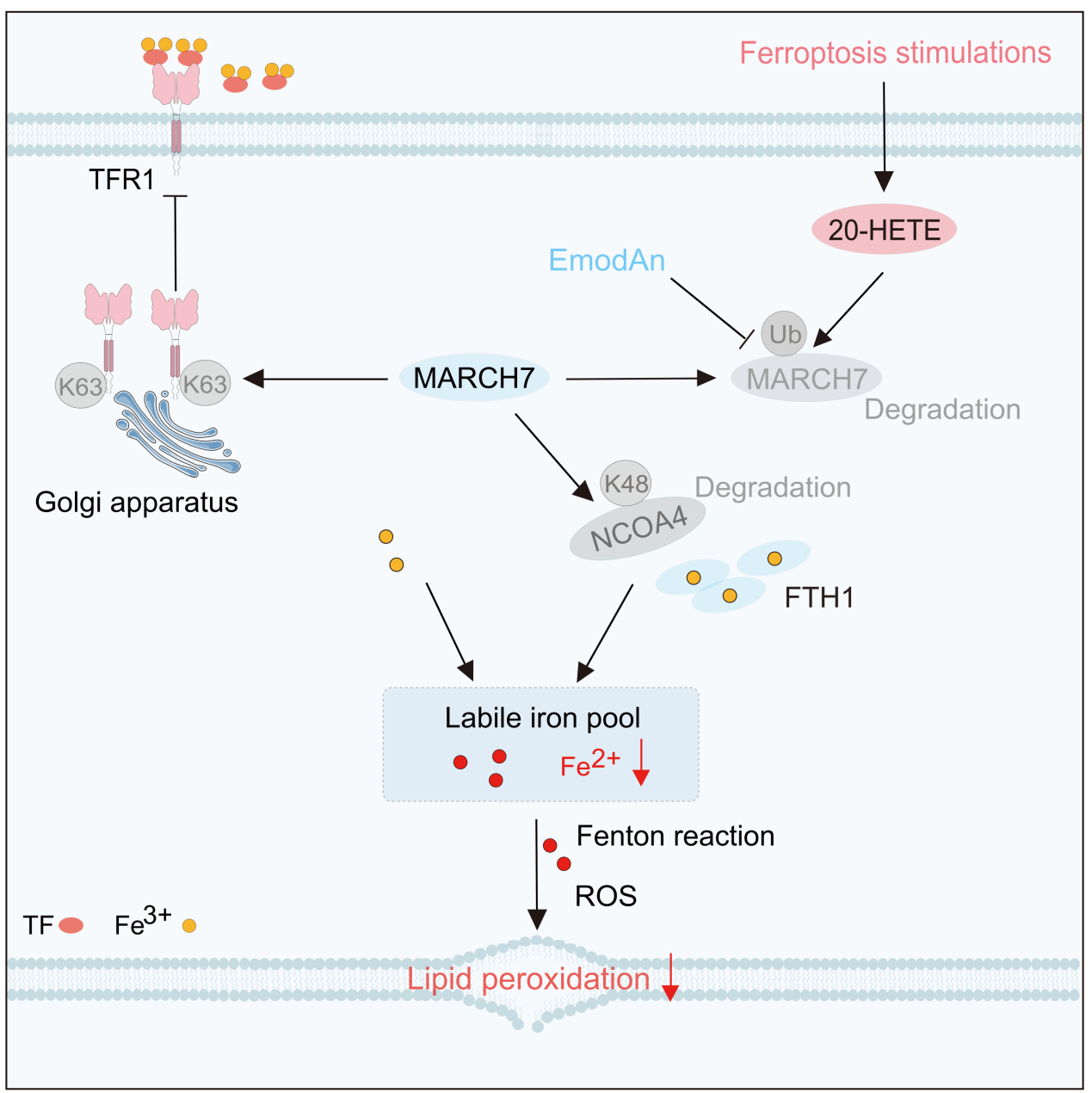
巴乾研究员基于前期已建立的多组学探究蛋白翻译后修饰和表达稳定性关系的研究策略和分析框架(Science Advances 2022,Developmental Cell 2021),和张强教授联合通过蛋白质组学与泛素化修饰组学的交叉研究,系统解析了铁死亡刺激下的细胞分子变化,发现E3泛素连接酶MARCH7是调控细胞铁稳态的核心枢纽和抵御铁死亡的“铁卫士”(ferro-guardian),并鉴定了其关键的泛素化底物蛋白。通过多团队合作,研究人员进一步明确了MARCH7通过双重泛素化机制实现对铁稳态的精细调控机制:一方面,MARCH7通过K48型泛素化修饰铁蛋白自噬受体NCOA4的K42位点,促进NCOA4降解,从而抑制铁蛋白自噬(Ferritinophagy)介导的细胞内铁释放;另一方面,MARCH7通过K63型泛素化修饰转铁蛋白受体TFR1的K53位点,抑制TFR1从内质网向细胞膜的转运,进而减少细胞对外部铁的摄取。这一“双向调控”机制,实现了对细胞铁稳态的全局把控。更为关键的是,研究发现,铁死亡刺激会诱导MARCH7自身发生泛素化降解,使其丧失对铁死亡的保护作用,形成放大铁死亡损伤的正反馈环路。
为发掘中药资源中的潜在靶向物质,研究人员进一步开发筛选探针并对天然产物库进行高通量筛选,最终发现来自中药大黄中的活性成分——大黄素蒽酮(EmodAn)——可特异性结合MARCH7蛋白,有效抑制铁死亡刺激诱导的MARCH7自身泛素化,稳定MARCH7蛋白水平,使其持续发挥铁稳态保护作用。在心肌缺血再灌注损伤疾病模型中,大黄素蒽酮展现出显著的心脏保护效应,有效改善心脏功能,为相关疾病的中医药干预提供了坚实的实验依据。
该研究是巴乾研究员团队开展“基于蛋白质功能状态的中药来源靶向药物研究”的重要成果,不仅补充了对铁死亡核心调控因子的认识,也证明了中药小分子可以特异性调控MARCH7实现对铁死亡的精准调控,具有显著的治疗潜力和转化前景,为中医药与现代生命科学的深度融合、特色中药创新药物研发提供了全新思路和重要支撑。
浙江大学张强教授、王福俤教授,我校巴乾研究员,浙江大学闵军霞教授,博观生物吴军兵博士为该文共同通讯作者。黄文祥、王睿君、杨鑫泉、杨双杰等学者为论文共同第一作者。研究得到国家自然科学基金、上海市东方英才拔尖计划、中国博士后面上基金和浙江大学基础医学院院长基金等多个科研项目支持。(科学技术处、附属市中医医院)