我校团队研发新型肾靶向Nrf2激动剂用于缓解急性肾损伤
发布时间:2025.07.26点击:10
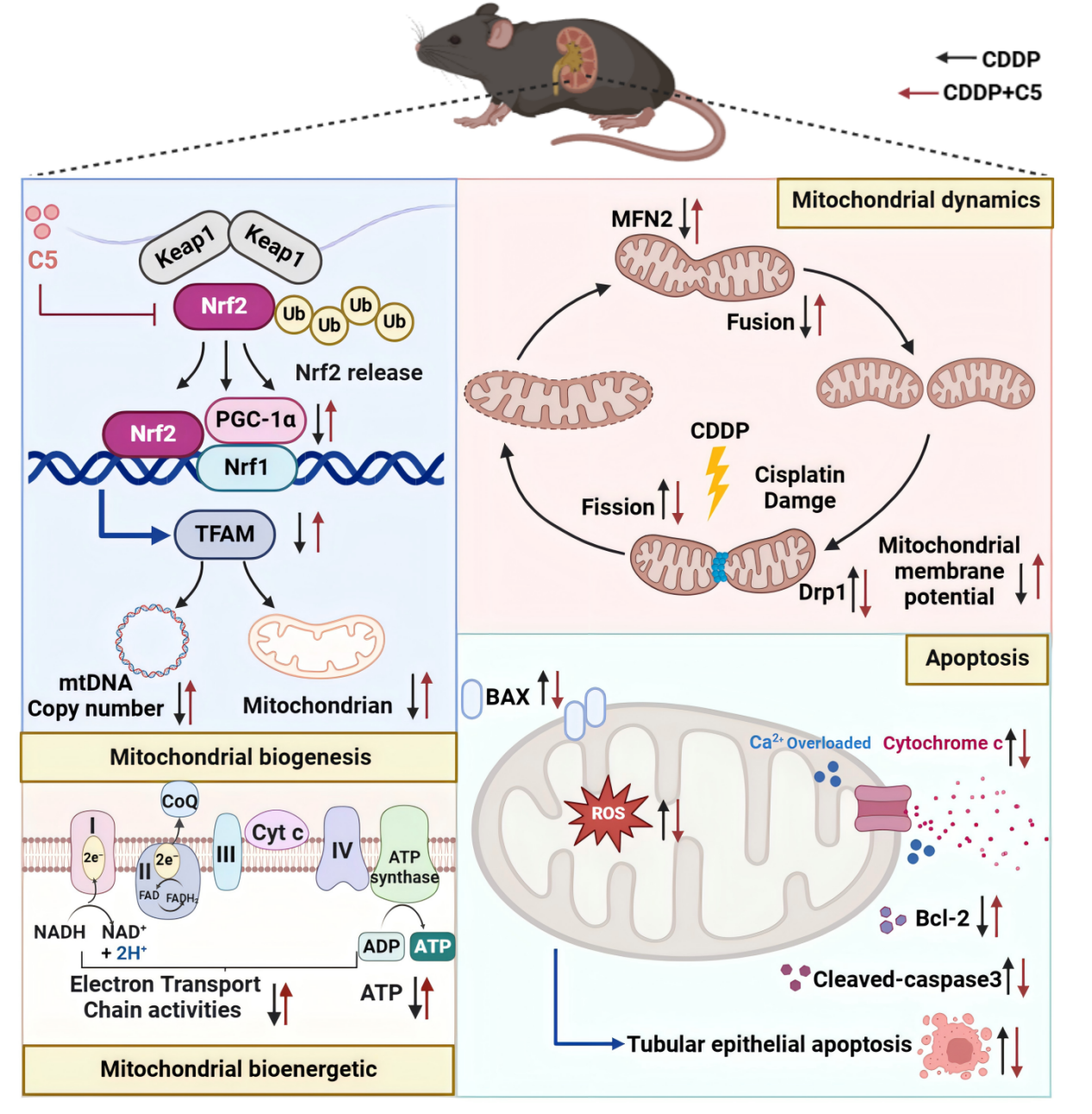
近日,我校交叉科学研究院葛广波教授团队与我校附属第七人民医院胡静主任团队合作,在国际权威学术刊物Redox Biology上在线发表题为“Discovery of a novel chalcone-derived covalent Keap1 binder for mitigating cisplatin-induced mitochondrial dysfunction and nephrotoxicity”的研究论文。该研究借助“高通量筛选-成药性优化-深度机制解析-多维度药效验证”的策略,成功研发一种新型肾靶向查尔酮衍生物C5。C5能够通过共价修饰Keap1的两个关键半胱氨酸位点(Cys288和Cys319),高效激活Keap1-Nrf2信号通路,从而显著改善顺铂诱导的线粒体功能障碍和肾损伤。该研究为开发高效、低毒的肾脏靶向肾损伤缓解药物提供了重要的候选分子和研究范式。

顺铂(Cisplatin, CDDP)是广泛应用于多种癌症(如卵巢癌、膀胱癌、肺癌等)治疗的基石化疗药物。然而,其严重的剂量限制性肾毒性极大制约了临床应用。研究表明,约21.4%的患者在接受顺铂治疗后会发生急性肾损伤,30%的患者会出现持续性肾功能下降。顺铂主要蓄积在肾脏近端小管细胞(PTCs),引发炎症、氧化应激、线粒体功能障碍和细胞凋亡等一系列级联反应,最终导致不可逆的肾损伤。线粒体作为细胞的“能量工厂”,其功能紊乱是顺铂肾毒性的核心环节。Keap1-Nrf2通路是细胞抵抗氧化应激和维持线粒体稳态的核心调控者,是开发肾保护剂的理想靶点。然而,现有Nrf2激动剂(如莱菔硫烷、巴多索隆等)存在代谢稳定性差、肾脏暴露量低、脱靶毒性等问题。
为解决这一难题,葛广波教授团队首先利用Nrf2-ARE荧光素酶报告基因系统对自建化合物库进行高通量筛选,发现查尔酮衍生物A6具有较强的Nrf2激活活性。随后,研究团队对A6进行了两轮系统的结构优化,并最终获得了综合性能最优的候选分子C5。C5表现出卓越的Nrf2激动活性、良好的代谢稳定性、安全性以及优异的细胞膜通透性。关键的是,C5展现出显著的肾脏靶向性。小鼠组织分布和质谱成像实验证实,C5在给药2小时后主要富集在肾皮质区域——这正是顺铂肾毒性的主要损伤部位。
进一步深度机制研究,C5能够选择性地共价修饰Keap1蛋白上的两个关键功能半胱氨酸:Cys288和Cys319。并且首次揭示Keap1上Cys319的变构调控可导致Keap1-Nrf2复合物解离。这种独特的双位点共价修饰机制使C5能够协同作用,阻断Keap1-Nrf2相互作用,促进Nrf2核转位,从而高效激活下游抗氧化(HO-1, NQO1, GCLC, GCLM)、抗炎、线粒体生物发生(PGC-1α/TFAM)和动力学平衡(MFN2/Drp1)等保护基因的表达。在进一步细胞模型和动物模型中,C5均可通过提升电子传递链复合物I-IV活性,恢复氧化磷酸化效率、促进线粒体生物发生(上调PGC-1α/TFAM)、恢复线粒体动力学平衡(上调融合蛋白MFN2,下调分裂蛋白Drp1)、稳定线粒体膜电位、抑制线粒体通透性转换孔开放等多维度协同调控改善顺铂诱导的线粒体功能障碍和肾损伤。
该研究相关成果已同步申请了国家发明专利,为研发新型肾脏保护剂提供研究示范。交叉科学研究院博士研究生邓言言、硕士研究生许雷志为论文共同第一作者,葛广波教授和附属第七人民医院胡静主任医师为论文共同通讯作者,上海中医药大学为论文的第一及通讯单位。该研究工作得到国家重点研发计划和国家自然科学基金等项目的支持。(科技处、交叉科学研究院)