交叉科学研究院葛广波团队在药物代谢酶特异性荧光底物研发领域取得新进展
发布时间:2025.05.28点击:268
近日,我校交叉科学研究院葛广波教授团队在国际权威学术刊物Chemical Science上在线发表题为“An optimized CYP3A4-activatable fluorogenic sensor for in situ functional imaging and multi-dimensional inhibitor assessment”的研究论文。该研究通过在荧光母体上引入类药基团,成功设计研发了口服可吸收的CYP3A4特异性荧光底物,在多种生物学维度下实现了CYP3A4活性的原位成像及其抑制剂的精准评估。

CYP3A4是人体最重要的药物代谢酶之一,其参与众多药物的代谢清除和代谢活化。长期以来,复杂生物体系中CYP3A4活性的检测主要依赖其药物底物和生理底物(如睾酮、咪达唑仑等)。CYP3A4药物/生理底物及其氧化产物的定量需借助液相色谱-质谱联用技术,该方法需要昂贵的设备和专业的操作人员,且样品前处理和分析过程相对耗时。相比之下,酶激活的荧光底物具有操作简单、响应快速、灵敏度高、适于高通量检测和原位超分辨率成像分析等优势,是开展目标酶亚细胞分布和功能检测的有力工具。但已报道的CYP3A4荧光底物多为P-糖蛋白(P-gp)的底物且无法口服吸收,严重制约了其在活体和活组织等复杂生物体系中的应用。因此,业界亟需研发口服有效且不受P-gp干扰的CYP3A4特异性荧光底物,进而用于复杂生命系统中CYP3A4的功能成像分析。
为此,该团队首先构建了一个CYP3A4激活的荧光底物库,通过整合计算机辅助虚拟筛选和P450酶反应表型分析发现N-环丙基甲基-1,8-萘酰亚胺(NCN)是理想的CYP3A4荧光底物,其表现出优异的同工酶特异性、超高的灵敏度、高亲和力、良好的细胞膜通透性,且NCN及其氧化代谢产物HNCN均不会被P-gp识别。NCN被成功于活细胞和活器官(离体)中CYP3A4活性的原位成像,进而评估生理状态和肝损伤状态下肝脏中的CYP3A4活性。动物整体实验研究表明:NCN具有良好的安全性和可接受的口服生物利用度(12.92%)。团队进一步借助NCN在多维度精确评估了抑制剂存在时CYP3A4的残余活性,发现CYP3A4抑制剂酮康唑可在重组单酶、组织制备物、活细胞、器官、活体等多维度抑制CYP3A4,进而显著提升NCN在大鼠体内的血浆暴露水平。
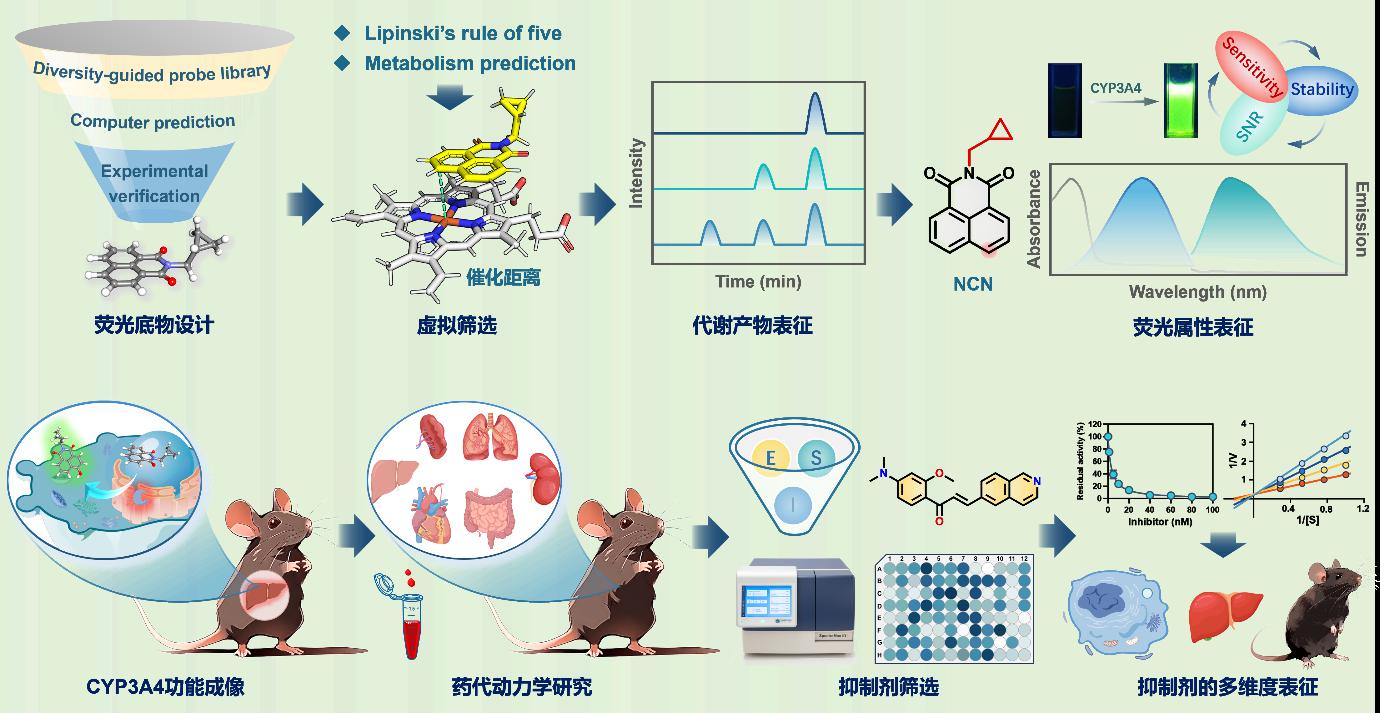
综上,该研究展示了一种计算机辅助分子设计和生化实验相结合的底物设计策略,该策略被用于CYP3A4亚型特异性荧光底物的理性设计。研究研发的NCN可作为一种实用且可靠的CYP3A4荧光底物,进而用于多种复杂生物体系中CYP3A4活性的原位成像及其抑制剂的多维度精准评价。相关工作已同步申请了国家发明专利。上述工作得到了英国巴斯大学Tony D. James教授在底物设计与合成方面的大力支持。我校交叉科学研究院博士后张凤和博士研究生范玉凡为论文共同第一作者,葛广波教授和Tony D. James教授为论文的通讯作者,上海中医药大学为本论文的第一及通讯单位。我校创新中药研究院杨笑迪研究员为荧光底物的分子轨道能级计算提供了技术支持和帮助。该研究工作得到国家重点研发计划和国家自然科学基金等项目的支持。(科技处、交叉科学研究院)